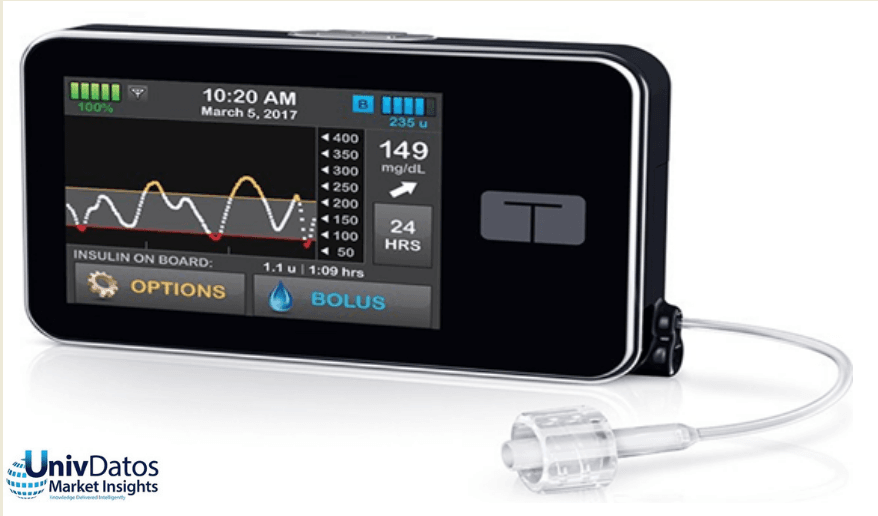
La FDA autoriza el T:Slim X2 de Tandem como la primera bomba de insulina "interoperable"
La diabetes, una afección que deteriora la capacidad del cuerpo para procesar la glucosa en sangre, es una de las enfermedades crónicas más comunes y costosas. El tratamiento intensivo de la glucosa, la presión arterial y los niveles de lípidos en personas con diabetes reduce sustancialmente el riesgo de desarrollar complicaciones relacionadas con la diabetes.
Recientemente, en febrero de 2019, la Administración de Alimentos y Medicamentos de EE. UU. ha otorgado la autorización de comercialización a la bomba de insulina t:Slim X2 con tecnología interoperable a Tandem Diabetes Care Inc. Hasta la fecha, las bombas de insulina han sido aprobadas por la FDA como parte de un sistema de gestión de la diabetes único y predefinido (dispositivos de clase III, de mayor riesgo) o autorizadas por la FDA como dispositivos independientes (dispositivos de clase II, de riesgo moderado). La bomba de insulina t:Slim X2 se ha revisado a través de la vía de revisión pre-comercialización de novo, ya que es interoperable con otros componentes de dispositivos para la diabetes.
Los avances en la salud digital han hecho posibles enfoques mucho más personalizados para la atención de la diabetes. Esta bomba t:Slim X2 funciona administrando insulina debajo de la piel a velocidades fijas o variables. Se puede conectar digitalmente y recibe comandos de dosificación de fármacos de otros dispositivos de gestión de la diabetes. Esto ha consolidado aún más el papel de Tandem Diabetes Care como un innovador clave en la industria de las bombas de insulina. Con este fin, lanzó la primera bomba con pantalla táctil aprobada como compatible con iCGM. Esta bomba es capaz de realizar actualizaciones de software de forma remota mediante el uso de una computadora personal, lo que ofrece a los usuarios la posibilidad de acceder a nuevas funciones a medida que cumplen con los requisitos reglamentarios necesarios.
t:slim X2 es al menos un 25 % más pequeña que todas las demás bombas de insulina duraderas disponibles en los Estados Unidos, y un 38 % más pequeña que el factor de forma de bomba de insulina más nuevo que ofrece uno de sus principales competidores. t:flex ofrece un factor de forma de bomba elegante similar, al tiempo que utiliza un cartucho con 480 unidades de insulina, lo que proporciona una mayor flexibilidad a las personas con mayores necesidades de insulina.
Hay más de un tercio de los adultos estadounidenses que tienen prediabetes y la mayoría de la población no está diagnosticada. Aproximadamente, 1 de cada 4 adultos vive con diabetes con alrededor de 7.2 millones de habitantes.
Según la American Diabetes Association, se estima que entre 750,000 y 1 millón de personas en todo el mundo usan una bomba de insulina. A nivel nacional, la compañía estima que aproximadamente 550,000 personas en los Estados Unidos usan una bomba de insulina, de las cuales aproximadamente el 80% tiene diabetes tipo 1. Esto indica la gran oportunidad para la bomba t:Slim X2 en el mercado de la diabetes.
Algunos de los actores clave en esta área incluyen a Roche (Accu-Chek Combo), Insulet Corporation (Omnipod), Medtronic (Minimed 530G System; 630G System) y Animas (Vibe).
