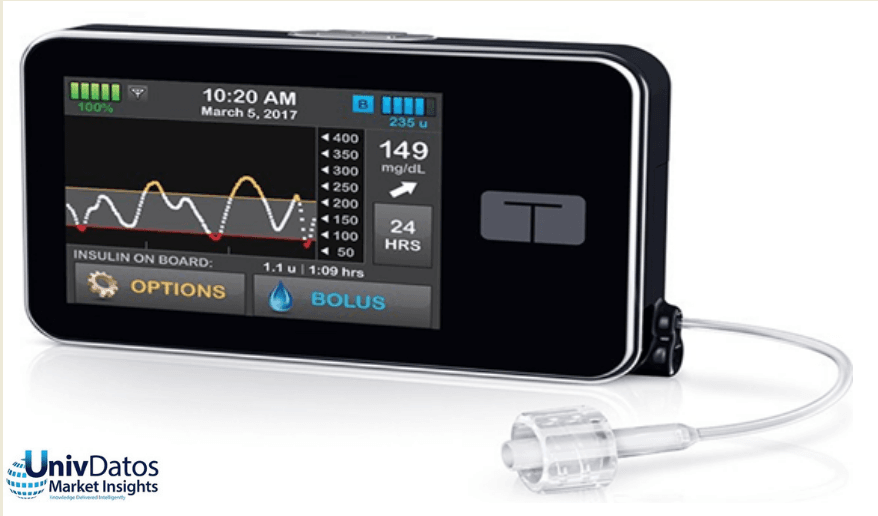
FDA、Tandem社のT:Slim X2を初の「相互運用可能」インスリンポンプとして承認
糖尿病は、体の血糖値を処理する能力を損なう疾患であり、最も一般的で費用のかかる慢性疾患の1つです。糖尿病患者のグルコース、血圧、脂質レベルを集中的に治療することで、糖尿病関連合併症を発症するリスクを大幅に軽減できます。
最近では、2019年2月に、米国食品医薬品局が、相互運用可能な技術を備えたt:Slim X2インスリンポンプの販売承認をTandem Diabetes Care Inc.に付与しました。現在まで、インスリンポンプは、単一の事前定義された糖尿病管理システム(クラスIII、最高リスクのデバイス)の一部としてFDAによって承認されているか、スタンドアロンデバイス(クラスII、中程度のリスクデバイス)としてFDAによって承認されています。t:Slim X2インスリンポンプは、他の糖尿病デバイスコンポーネントと相互運用可能であるため、デノボ事前市場審査経路を通じて審査されています。
デジタルヘルスの進歩により、糖尿病ケアに対するより個別化されたアプローチが可能になりました。このt:Slim X2ポンプは、設定された速度または可変速度で皮膚の下にインスリンを投与することによって機能します。デジタルで接続でき、他の糖尿病管理デバイスから薬物投与コマンドを受信できます。これにより、Tandem Diabetes Careのインスリンポンプ業界における主要なイノベーターとしての役割がさらに確立されました。この目的のために、iCGM互換として承認された最初のタッチスクリーンポンプを発売しました。このポンプは、パーソナルコンピュータを利用してリモートソフトウェアアップデートが可能であり、ユーザーが必要な規制要件を満たすと、新機能にアクセスできる可能性があります。
t:slim X2は、米国で入手可能な他のすべての耐久性のあるインスリンポンプよりも少なくとも25%小さく、主要な競合他社の1つが提供する最新のインスリンポンプフォームファクタよりも38%小さくなっています。t:flexは同様の洗練されたポンプフォームファクタを提供しながら、480単位のインスリンを含むカートリッジを利用し、より多くのインスリンを必要とする人々に強化された柔軟性を提供します。
米国成人の3分の1以上が糖尿病予備群であり、人口の大部分は診断されていません。およそ、成人の4人に1人が糖尿病を患っており、約720万人の人口がいます。
米国糖尿病協会によると、世界中で75万人から100万人がインスリンポンプを使用していると推定されています。国内では、米国で約55万人がインスリンポンプを使用しており、そのうち約80%が1型糖尿病であると推定されています。これは、糖尿病市場におけるt:Slim X2ポンプの大きな機会を示しています。
この分野の主要なプレーヤーには、Roche(Accu-Chek Combo)、Insulet Corporation(Omnipod)、Medtronic(Minimed 530G System; 630G System)、Animas(Vibe)が含まれます。
