报告的主要亮点:
- 医疗保健领域的需求不断增长:由于对广泛的药物成瘾病例日益关注,医疗保健领域的需求不断增长,使得复方新诺明市场正经历着显著的增长。
- 医药市场崛起:由于艾滋病毒/艾滋病的发病率增加,对药品的需求不断增长。
- FDA 批准时间表:品牌和仿制药复方新诺明的 FDA 批准时间表。
根据 Univdatos Market Insights 的一份新报告,复方新诺明市场预计到 2030 年将达到百万美元,复合年增长率为 3%。复方新诺明是拉米夫定和齐多夫定这两种药物的组合的商品名,用于治疗人类免疫缺陷病毒/获得性免疫缺陷综合征。这些药物充当抗逆转录病毒剂,通过竞争性抑制和降低逆转录酶的活性来对抗 HIV。复方新诺明通常用于对抗人类免疫缺陷病毒。在考虑类型时,由于其成本效益,与品牌药物类型相比,仿制药类型占据了最大的份额。包括药物成瘾病例的增加、对艾滋病毒/艾滋病相关宣传计划的激增以及医疗保健部门投资的增加等多种因素正在推动复方新诺明的增长。除了这些因素外,用于 HIV 治疗的战略合作的增加正在引领预测期内复方新诺明市场的发展。例如,2023 年 6 月,总部位于美国的 A-Alpha Bio 与 Gilead 合作,以加强 HIV 治疗选择。
在此处访问 PDF 样本 - https://univdatos.com/get-a-free-sample-form-php/?product_id=49099
该报告表明,仿制药的推出和批准数量的增加是未来几年推动复方新诺明市场增长的主要因素之一。复方新诺明仿制药的开发在制药行业的研发方面获得了支持。资金是在市场上获得突出地位的重要因素,而 HIV 治疗研究正在吸引大量的资金投入。这笔支出正在推动更有效且更节省成本的新型复方新诺明仿制药的开发市场。近年来,在 FDA 批准方面,新药推出数量不断增加,并且越来越多地关注艾滋病毒/艾滋病的技术进步,以及多项控制 HIV 传播的政府举措。例如,总部位于美国的美国卫生与公众服务部 (HHS) 于 2019 年启动了一项名为“结束 HIV 流行病 (EHE)”的计划,其宏伟目标是到 2030 年将美国所有新的 HIV 感染减少 90%。HHS 还为各个司法管辖区提供了多种资金机会,包括对性传播疾病专科诊所的同步投资。它还为患者通过复方新诺明获得更好的护理和支持提供了希望,并且可以作为未来提供更好的治疗选择的门户。
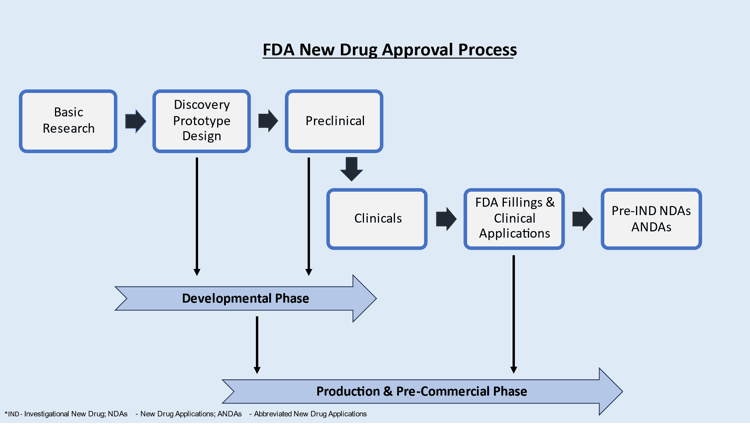
复方新诺明 FDA 批准时间表:所有品牌和仿制药拉米夫定/齐多夫定制剂用于复方新诺明形成的 FDA 批准历史。
品牌药:
1997 年 -
- 复方新诺明片剂;口服 (150mg;300mg)
活性成分:拉米夫定;齐多夫定
申请人:ViiV Healthcare(英国)
仿制药:
2011 年 -
- 拉米夫定和齐多夫定片剂;口服 (150mg;300mg)
申请人:Chartwell Rx(美国)
2012 年 -
- 拉米夫定和齐多夫定片剂;口服 (150mg;300mg)
申请人:Aurobindo Pharma Ltd(印度)
- 拉米夫定和齐多夫定片剂;口服 (150mg;300mg)
申请人:Lupin Ltd(印度)
2014 年 -
- 拉米夫定和齐多夫定片剂;口服 (150mg;300mg)
申请人:Hetero Labs Ltd V(印度)
2015 年 -
- 拉米夫定和齐多夫定片剂;口服 (150mg;300mg)
申请人:Strides Pharma(印度)
- 拉米夫定和齐多夫定片剂;口服 (150mg;300mg)
申请人:Hetero Labs Ltd III(印度)
2017 年 -
- 拉米夫定和齐多夫定片剂;口服 (150mg;300mg)
申请人:PharmaCare(澳大利亚)
- 拉米夫定和齐多夫定片剂;口服 (150mg;300mg)
申请人:Aurobindo Pharma(印度)
2018 年 -
- 拉米夫定和齐多夫定片剂;口服 (150mg;300mg)
申请人:Anda Repository(美国)
- 拉米夫定和齐多夫定片剂;口服 (150mg;300mg)
申请人:Macleods Pharms Ltd(印度)
- 拉米夫定和齐多夫定片剂;口服 (150mg;300mg)
申请人:Cipla(印度)
2019 年 -
- 拉米夫定和齐多夫定片剂;口服 (150mg;300mg)
申请人:Mylan Labs Ltd(印度)
结论
全球复方新诺明市场是一个快速增长的领域,技术进步正在改善 HIV/艾滋病患者的治疗效果。随着新技术的开发,预计未来几年全球复方新诺明市场将继续增长。总体而言,全球复方新诺明市场为制药行业提供了重要的机会,制药行业正在建立战略联盟,以设计一种有效的艾滋病治疗药物。随着持续的研发,未来可能会有更多的治疗方法出现,从而通过复方新诺明改善患者的治疗效果。
获取回电
